Рассматривает возможность протекания реакций алканов, сопровождающихся отщеплением части молекулы. Как называются подобные реакции?
При нагревании до температуры выше 500° в молекулах алканов происходит разрыв связей между атомами углерода. И могут образоваться углеводороды с меньшей молярной массой. Не только алканы, но и алкены. Этот процесс называется термическим крекингом (от англ. tocrack– «колоть, расщеплять»).
C 10H22---------C5H12+C5H10
C10H22---------C4H10+C6H12
В результате крекинга образуется смесь алканов и алкенов с меньшим количеством атомов углерода в молекулах, чем у исходного углеводорода. Чем выше температура крекинга, тем более легкие углеводороды образуются в результате.
В настоящее время в промышленности крекинг проводят чаще всего, используя катализаторы. В качестве катализаторов обычно применяют алюмосиликаты.
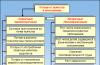
Каталитический крекинг протекает при более низких температурах, чем термический, и при этом происходит не только простое расщепление углеводородов, но и перестройка их углеродного скелета или изомеризация. В результате образуются углеводороды с более разветвлённым скелетом, чем исходные.
(каталитический крекинг – схема)
Это важно для повышения качества топлива. Каталитический крекинг углеводородов нефти – один из промышленных способов повышения октанового числа бензина. При увеличении температуры можно достичь такой степени протекания реакции, при которой органические вещества – углеводороды – полностью разлагаются на углерод и водород. Такой процесс называется пиролизом.
При пропускании нагретого алкана над платиновым или никелевым катализатором может отщепиться водород. Этот процесс называется дегидрированием.
В результате этой реакции получаются непредельные углеводороды - алкены. Есть еще один важный процесс, при котором алканы, содержащие более 6 атомов углерода, нагревают над сложным катализатором. Этот катализатор обычно состоит из алюмосиликатов с добавкой платины. В результате отщепляется водород и образуются ароматические углеводороды – арены. Такой процесс называют риформингом
Его, так же, как и крекинг, используют в промышленности для получения бензина с высоким октановым числом.
Есть еще важная для промышленности реакция алканов – конверсия.
СН4+Н2O CO+3H2
Так называют взаимодействия алканов, из которых чаще всего используют природный газ с парами воды. При высокой температуре около 1000 образуется смесь оксида углерода – угарного газа и водорода. Эту смесь называют синтез газ. Часто ее не разделяют, а используют для получения разных органических веществ.
все возможные продукты. Реакция бромирования алканов – селективная, т.к. образуются далеко не все возможные продукты.
Бромирование алканов
Вернуться к содержанию
CH4 + Br2===CH3Br + HBr механизм реакции «Sr». Аналогично: CH3-CH3+ Br2=== CH3-CH2Br + HBr. Йод же с алканами реагирует очень медленно или не реагирует вообще. Реакция является обратимой и практического значения не имеет.
Селективность реакций хлорирования и бромирования алканов
Продолжить просмотр химических свойств
В случаях хлорирования и бромирования простых линейных алканов данный вопрос не актуален, т.к. основной продукт реакции только один… Если же мы рассмотрим реакции хлорирования и бромирования н-пропана, то обнаружим существенные различия: в случае хлорирования пропана в качестве продуктов мы получим 1-хлорпропан и 2-хлорпропан, т.е. хлор будет замещать атом водорода у первого и у второго атома углерода; в случае же бромирования пропана Br будет замещать водород только у второго атома С… Такая тенденция будет наблюдаться и при дальнейшем увеличении цепи реагирующего алкана. Cl соединяется со всеми радикалами, а бром только с самым устойчивым радикалом (который существует дольше по времени). Это объясняется их различной химической активностью, бром более «медлительный» и хуже вступает в соединение. В случае с пропаном бром соединился с более устойчивым вторичным радикалом.
Слайд 1
Описание слайда:
Слайд 2

Описание слайда:
Слайд 3

Описание слайда:
Слайд 4

Описание слайда:
Слайд 5

Описание слайда:
Слайд 6

Описание слайда:
Слайд 7

Описание слайда:
Слайд 8

Описание слайда:
Слайд 9

Описание слайда:
Слайд 10

Описание слайда:
Слайд 11

Описание слайда:
Слайд 12

Описание слайда:
Слайд 13

Описание слайда:
Слайд 14

Описание слайда:
Слайд 15

Описание слайда:
Слайд 16

Описание слайда:
Слайд 17

Описание слайда:
Слайд 18

Описание слайда:
Слайд 19

Описание слайда:
Слайд 20

Описание слайда:
Слайд 21

Описание слайда:
Слайд 22

Описание слайда:
Слайд 23

Описание слайда:
Слайд 24

Описание слайда:
Слайд 25

Описание слайда:
Слайд 26

Описание слайда:
Слайд 27

Описание слайда:
Слайд 28

Описание слайда:
Слайд 29

Описание слайда:
Слайд 30

Описание слайда:
Слайд 31

Описание слайда:
Слайд 32

Описание слайда:
Слайд 33

Описание слайда:
КАРБОНОВЫЕ КИСЛОТЫ Карбоновые кислоты - органические соединения, молекулы которых содержат одну или несколько карбоксильных групп -СООН, связанных с углеводородным радикалом. Изучение карбоновых кислот лучше начинать с рассмотрения одноосновных насыщенных кислот, общая формула которых Сп Н2п+1СООН. Карбоновые кислоты бывают одноосновные или монокарбоновые; по характеру углеводородного радикала различают предельные, непредельные и ароматические кмслоты. Названия карбоновых кислот по систематической номенклатуре производчт от названия предельных углеводородов с добавлением окончания –овая и слова кислота.Нумерацич главной цепи начинается с углерода, входящего в состав карбоксильной группы.
Слайд 35

Описание слайда:
Слайд 36

Описание слайда:
Слайд 37

Описание слайда:
Сложные эфиры, R-COOR" - производные карбоновых кислот, в которых гидраксильная группа –ОН карбоксила замещена на группу OR‘. Их получают при взаимодействии карбоновой кислоты со спиртом (катализатор – сильная кислота): Сложные эфиры, R-COOR" - производные карбоновых кислот, в которых гидраксильная группа –ОН карбоксила замещена на группу OR‘. Их получают при взаимодействии карбоновой кислоты со спиртом (катализатор – сильная кислота): Образование сложного эфира из кислоты и спирта называется реакцией этерификации. Это обратимый процесс. Обратная реакция - гидролиз сложного эфира. Установлено, что при этерификации от кислоты отщепляется гидроксил, а от спирта водород (т.е. спирт выступает в качестве нуклеофила, образуя связь с карбонильным атомом углерода за счет своей неподеленной электронной пары). Амиды (R-CONH2) – производные карбоновых кислот, в которых гидроксильная группа –ОН замещена на аминогруппу –NH2. Амиды получают при взаимодействии кислот с аммиаком при нагревании для разложения образующейся аммониевой соли.
Описание слайда:Аминокислоты Аминокислоты - органические соединения, содержащие в молекуле два типа функциональных групп: карбоксильную -СООН, и аминогруппу -NН2, т.е относится к гетерофункциональным соединениям. Аминокислоты можно также рассматривать как производные карбоновых кислот, содержащих в радикале одну или несколько аминогрупп. Аминокислоты играют огромную роль в жизни животных и растительных организмов, так как являются теми структурными элементами, из которых построены молекулы важнейшего природного полимера - белка - основы всего живого. Классифицируются аминокислоты по взаимному расположению функциональных групп, по числу и характеру функциональных групп, по химической природе радикала R -аминокислот. Для аминокислот применима международная номенклатура (ИЮПАК), но чаще используют тривиальные названия. Тривиальные названия -аминокислот обычно связаны с источником выделения.
Слайд 41

Описание слайда:
Слайд 42

Описание слайда:
С катионами тяжелых металлов а -аминокислоты как бифункциональные соединения, образуют внутрикомплексные соли, например, со свежеприготовленным гидроксидом меди (П) в мягких условиях получаются хорошо кристаллизующиеся хелатные С катионами тяжелых металлов а -аминокислоты как бифункциональные соединения, образуют внутрикомплексные соли, например, со свежеприготовленным гидроксидом меди (П) в мягких условиях получаются хорошо кристаллизующиеся хелатные соли меди (П) синего цвета (от греч. "хела" - клешня). Эти комплексы хорошо растворимы в воде, в некоторых органических растворителях и широко используются для обнаружения - аминокислот в аналитической химии. Благодаря своей амфотерности аминокислоты в живом организме играют роль буферных веществ, поддерживающих определенную концентрацию водородных ионов.
Слайд 43

Описание слайда:

Алканы – углеводороды с общей формулой: С n H 2n+2 ,
в молекулах которых атомы связаны одинарными связями.

Метан
Пропан
Этан
Бутан
Структурная формула пропана

S Р 3 – гибридизация
Валентный угол -109 о 28
Тетраэдр
Длина углерод – углеродной связи: 0,154 нм


Алканы с большим числом атомов углерода имеют зигзагообразное строение
Модель молекулы пентана

Различия в порядке соединения атомов в молекулах (т. е. в химическом строении) приводят к структурной изомерии . Строение структурных изомеров отражается структурными формулами. В ряду алканов структурная изомерия проявляется при содержании в цепи 4-х и более атомов углерода, т. е. начиная с бутана С 4 Н 10 .
С С
С С С С С С С С
С С
2,2 диметилбутан
2,3 диметилбутан

Все алканы плохо растворимы в воде. С ростом молекулярной массы закономерно увеличиваются температуры кипения и плавления.
Начиная с гексадекана появляются твёрдые алканы.

1 – выделение углеводородов из природного сырья
2- гидрирование циклоалканов и непредельных углеводородов
4- синтез Вюрца
5- гидролиз карбидов

Реакции гидрирования
Циклоалканов:
С 5 Н 8 + Н 2 = С 5 Н 10
Алкинов:
С 2 Н 2 + 2Н 2 = С 2 Н 6
Алкенов:
С 2 Н 4 + Н 2 = С 2 Н 6
Алкадиенов:
С 4 Н 6 + 2Н 2 = С 4 Н 10
+ Н 2

Получение метана при сплавлении ацетата натрия со щелочью :
CH 3 COONa + NaOH CH 4 + Na 2 CO 3
ацетат натрия метан
Свойства метана:
1) метан не вступает в реакцию окисления при действии водного раствора KMnO 4 ;
2) метан не вступает в реакцию с раствором брома;
3) горение метана:
CH 4 + 2О 2 СО 2 + 2Н 2 О + Q

Синтез Вюрца
проводят с целью получения алканов с более длинной углеродной цепью.
Например: получение этана из метана
1 этап. Галогенирование исходного алкана
СН 4 + С l 2 = CH 3 Cl + HCl
2 этап. Взаимодействие с натрием
2CH 3 Cl + 2 Na = C 2 H 6 + 2NaCl

Метан в лаборатории можно получить гидролизом карбида алюминия
Al 4 C 3 + 12 H 2 O = 4 Al(OH) 3 + 3 CH 4

1- реакции замещения
2- реакции дегидрирования
3- реакции горения
4 - реакции изомеризации
5- термическое расщепление

Хлорирование метана:
CH 4 + Cl 2 = CH 3 Cl +HCl
CH 3 Cl + Cl 2 = CH 2 Cl 2 +HCl
CH 2 Cl 2 + Cl 2 = CHCl 3 + HCL
CHCl 3 + Cl 2 = CCL 4 + HCL
Пример реакции замещения:
Взаимодействие декана с бромом
С 10 Н 22 + Br 2 = С 10 Н 2 1 Br + HBr

При дегидрировании алканов образуются алкены и другие непредельные углеводороды.
Например, дегидрирование пентана:
С 5 Н 10 С 5 Н 8 + Н 2
пентен

Все алканы горят с образованием углекислого газа и воды
Например: горение бутана
2С 4 Н 10 + 13О 2 = 8СО 2 + 10Н 2 О

Реакции изомеризации идут при нагревании и в присутствии катализатора
Например: изомеризация пентана (с хлоридом алюминия)
СН 3 -СН 2 -СН 2 -СН 2 -СН 3 СН 3 -СН-СН 2 -СН 3
СН 3

Термическое расщепление
1- крекинг (400-500 о С)
Алкан новый алкан и алкен
С 20 Н 42 С 10 Н 22 + С 10 Н 20
2- пиролиз метана при 1000 о С
СН 4 С + 2Н 2
3- получение ацетилена при нагревании до 1500 о С
2СН 4 С 2 Н 2 + 3Н 2

Получение растворителей
Получение ацетилена
А также сырьё для синтезов спиртов, альдегидов, кислот.
Горючее для дизельных и турбореактивных двигателей
В металлургии


- Какие углеводороды относят к алканам?
- Запишите формулы возможных изомеров гексана и назовите их по систематической номенклатуре.
- Напишите формулы возможных продуктов крекинга октана
4. В каком объёмном соотношении смесь метана с воздухом становится взрывоопасной?
5. Каковы природные источники получения алканов?
6. Назовите области применения алканов
ТЕСТ

ОТВЕТЫ К ТЕСТУ: